2020年2月,国家药品监督管理局(NMPA)共批准首次注册的医疗器械产品170个。对这些产品数据进行系统性的分析与处理,有助于洞察我国医疗器械行业的创新动态、技术发展趋势及监管重点。
一、数据概况与来源
本次分析的数据来源于NMPA官方网站2020年2月发布的首次注册产品公告。原始数据字段通常包括:产品名称、注册人名称、注册人住所、管理类别、分类编码、结构及组成/产品描述、适用范围/预期用途、规格型号、批准日期及注册证编号等。
二、数据处理流程
- 数据清洗:对原始数据进行标准化处理,统一命名规范(如公司名称全称与简称的归一化),处理缺失值与异常值,确保数据的一致性与准确性。
- 数据归类与编码:依据《医疗器械分类目录》,对产品的管理类别(Ⅰ、Ⅱ、Ⅲ类)和分类编码进行核对与标准化,这是后续统计分析的基础。
- 关键信息提取:从“结构及组成”和“适用范围”中提取关键技术特征(如是否含药、是否可吸收、是否软件驱动等)和临床用途领域,为深度分析做准备。
三、核心数据分析维度
- 管理类别分布:分析170个产品中Ⅰ类、Ⅱ类、Ⅲ类产品的数量及占比。数据显示,Ⅱ类医疗器械占据绝对主导(约70%),反映了市场以中等风险产品创新为主的格局;Ⅲ类高风险产品数量相对较少(约15%),但其技术含量和临床价值通常更高;Ⅰ类产品(约15%)多为备案制,体现了简政放权的监管思路。
- 技术领域分布:通过对分类编码的统计分析,可以揭示热点技术领域。2020年2月,注册产品可能集中在外科器械、医用成像器械、临床检验器械、骨科植入物等领域。例如,“有源手术器械”、“无源植入器械”、“医用软件”等子领域的产品数量值得关注。
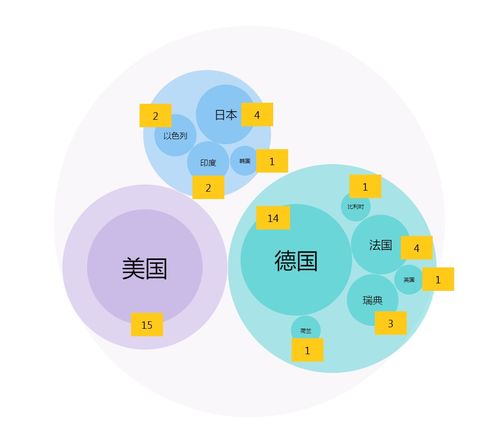
- 注册人地域分析:对注册人住所进行地理信息分析,可以勾勒出我国医疗器械产业的区域分布图。通常,长三角、珠三角及京津冀地区的企业创新能力突出,注册产品数量领先,显示出产业集聚效应。
- 产品特性分析:通过文本分析“适用范围”,可统计产品主要针对的疾病领域(如心血管、骨科、眼科、肿瘤等)和治疗目的(诊断、治疗、监测、康复等)。识别是否包含人工智能、远程监测、可降解等新兴技术元素,能评估行业技术前沿动向。
四、分析结论与洞察
- 产业创新活跃:单月170个首次注册产品,表明我国医疗器械产业研发与创新转化活跃,企业持续投入新产品开发。
- 风险管控审慎:产品结构以Ⅱ类为主,符合风险分级管理的原则,在鼓励创新与控制风险之间取得了平衡。
- 技术升级明显:数据分析可能显示,涉及数字化、智能化、微创化、精准化的产品占比呈上升趋势,体现了产业技术升级的方向。
- 区域发展不均衡:优势区域的产业集中度可能较高,提示需加强其他地区的产业政策引导与创新能力培育。
五、数据处理的价值与应用
对NMPA首次注册数据的系统处理与分析,具有多重价值:
- 对于监管机构:可动态监测产品上市趋势,评估审评审批效能,为优化监管政策提供数据支撑。
- 对于医疗器械企业:可洞察竞争格局、技术热点与市场空白,辅助研发立项与战略决策。
- 对于投资与研发机构:可识别高成长性技术赛道与创新型企业,指引投资与科研方向。
- 对于医疗机构:可了解新产品上市动态,为临床新技术、新设备的引进提供信息参考。
对2020年2月NMPA首次注册的170个产品数据进行科学的处理与分析,不仅能够清晰描绘当月的产品注册全景,更能深度挖掘背后的产业趋势、技术路径与政策导向,为相关各方提供有力的决策支持。随着数据量的积累,进行时间序列的对比分析(如同比、环比),将能进一步揭示行业发展的长期规律与周期性特征。